leky-latky/acidobazicka-rovnovaha/krev-plazma-a-ABR
Anion gap
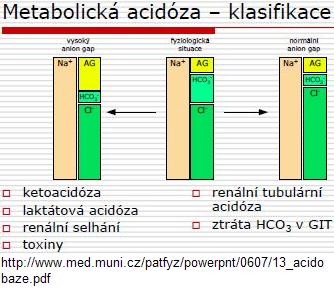
- AG = Na+ – (Cl- + HCO3-)
- AG = [Na+] - [Cl-] - [HCO3-]
- Cca 12 - 15
- Je podstatné, zda je snížení sérové koncentrace HCO3- spojeno se
- Zvýšením sérové koncentrace chloridů
- Neschopností vstřebávat HCO3 ledvinami - kompenzace zvýšením Cl-
- Aj.
- Zvýšením koncentrace jiných aniontů - kompenzované zvýšeným vylučováním HCO3 / vydýcháváním CO2
Zvýšení AG + pokles HCO3- a
- Hromadění běžně neměřených aniontů kyselin
- Ketokyselin
- Acetoacetát
- Laktátu
- Sulfát
- Toxických látek aj. v extracelulární tekutině (ECT)
- Negativně nabité proteiny
- Cca 10% plazmatických aniontů
AG korekce na sérovou koncentraci albuminu
- AG korig = AG + 0,25 × (40 – S alb)
- Elektrický náboj nesený albuminem není zanedbatelný
- Především v případech hypoalbuminemie současně s retinovanými anionty silných kyselin
- Bez korekce na albumin dochází k falešně nízkým hodnotám AG
- www.prolekare.cz/casopisy/vnitrni-lekarstvi/2016-suppl-6/metabolicka-acidoza-u-chronickeho-onemocneni-ledvin-60094
Base excess - BE
Srovnávání
- Založen na stanovení primární změny, pCO2 vs [HCO3-]
- Všechny základní acidobazické poruchy mají charakteristickou HCO3-/pCO2 hodnotu
- Diagnóza acidobazické poruchy může být stanovena na základě srovnání skutečné hodnoty v HCO3-/pCO2 daného pacienta s hodnotou očekávanou
- Avšak součástí změny sérové koncentrace HCO3- je i posun v rovnovážné reakci HCO3--CO2 v důsledku kompenzační ventilační reakce (změna pCO2)
- U pacientů s metabolickou acidobazickou poruchou [7]
Siggaard-Andersenův hodnocení base excess (BE)
- Množství kyseliny nebo zásady, které musí být přidáno do krve in vitro pro obnovení pH na hodnotu 7,40
- Zatímco pCO2 je udržován na hodnotě 40 mm Hg [7]
- Tím byl téměř eliminován efekt respirační kompenzace ovlivňující hodnocení metabolické komponenty ABR
- Zároveň byl vzat v úvahu významný krevní pufr – hemoglobin
- V současné době pravděpodobně nejrozšířenější metodou hodnocení ABR v klinické praxi
HCO3- - CO2
- Je v rovnováze s nebikarbonátovými pufry
- Vztah mezi celkovou koncentrací protonových akceptorů X aktivita volných protonů ve vodném roztoku
- Ke změnám koncentrace HCO3- a pCO2 z důvodu
- Změny jejich hmotnostní bilance
- Posunu v HCO3--CO2 rovnovážné reakci [7]
pH Kreve arteriální krve
- 7,40 ± 0,02
- [H+] = 38–42 nmol/l [2]
- Možný život
- 6,8–7,8 ± 0,1
- [H+] = 10–160 nmol/l [2]
- PH arteiální krve vyšší o cca 0.5 až 0.6 pH než intracelulární pH
- Zhruba 4-násobný gradient
- Usnadňuje přestup H+ z buňky
- Pokles arteriálního pH ze 7,4 na cca 6,9 - 6,8 = zhoršený přestup H+ z buněk do krve !!!
- Přesnější než hodnoty venózní krve
- Ty jsou více proměnlivé dle metabolických nároků jednotlivých tkání
Base excess (nebo deficit) - BE
- HCO3- vzestup nebo pokles
- Množství fixní kyseliny nebo báze, která musí být přidána k 1 litru krve nasycené kyslíkem při PCO2 40 torrů (5,32 kPa), aby se pH vrátilo k normě (tj. 7,4) [2]
- Normální hodnoty jsou ± 2,3 mmol/l [2]
Buffer base – BB - sdružené nárazníkové báze
- Celkové množství nárazníkových zásad, které mohou přijímat H+ v krvi
- Normální hodnoty 46–52 mmol/l krve nasycené kyslíkem [2]
Natrio-chloridová diference - diference [Diff(NaCl)]
Pokles
- Diluční efekt
- účast či spoluúčast poruchy natrio-chloridového metabolizmu
- Např: koncentrace Na+ a Cl- jsou ještě v referenčním rozmezí
- AG zvýšena
- Diff(NaCl) je již snížena
- Ionty Na+ a Cl- mají velmi široké referenční rozmezí
- Na+ 137–146 mmol/l
- Cl- 97–108 mmol/l
- Např. Na+ 137 mmol/l mínus Cl- 108 mmol/l
- Diff(NaCl) je rovna 29 mmol/l
- Může dojít k poklesu [Na+-Cl-] diference až o 8 mmol/l, považujeme-li za střední hodnotu Diff(NaCl) 37 mmol/l
Vztah mezi [HCO3-], [Na+-Cl-] z výpočtu AG:
- AG = Na+ – (Cl- + HCO3-), který můžeme upravit do tvaru
- AG = (Na+ – Cl-) – HCO3-, vyjádříme-li HCO3-
- HCO3- = (Na+ – Cl-) – AG
- Pokud se AG významněji nemění
- Musí existovat lineární vztah mezi sérovou koncentrací HCO3- a [Na+-Cl-]
- Pokles Diff(NaCl) z 37 na 29 mmol/l při normální hodnotě AG
- Tedy odráží pokles sérové koncentrace bikarbonátu z 24 na 16 mmol/l
- Může upozornit na přítomnost středně těžké metabolické acidózy v důsledku ztrát bikarbonátu, nicméně bez očekávané hyperchloremie
- V případě že hodnota [Na+-Cl-] zůstává přibližně konstantní
- Bude existovat nepřímý lineární vztah mezi HCO3- a AG.
- Diff(NaCl) je klinicky velmi přínosný, snadno dostupný parametr
- Odchylky jednotlivých iontů Na+ a Cl- jsou zcela běžné
- Jejich rozdíl však, dle naší zkušenosti, zůstává bez současné poruchy ABR obyčejně zachován
- Samotný pokles Diff(NaCl), bez znalosti acidobazických parametrů
- Nás může upozornit na metabolickou acidózu s normálním AG
- Mohou tak být odkryty poruchy ABR spojené se ztrátou HCO3-
- Např. renální tubulární acidózy, ještě bez poklesu GFR
- V případě gastrointestinálních ztrát HCO3-
- Můžeme dle poklesu Diff(NaCl) odhadnout stupeň metabolické acidózy
- U metabolické acidózy, pouze na základě retence kyselin, samozřejmě Diff(NaCl) zůstává nezměněna
Zvýšená Diff(NaCl)
- Může upozornit na všechny typy metabolické alkalózy, které bývají spojeny s
- Hypochloremií
- Ev. hypernatremií
- Systematické zhodnocení vztahu mezi Diff(NaCl) a HCO3- u jednotlivých poruch ABR
pH smíšené venózní krve
- Nižší o 0,02–0,05 pH než arteriální krve [2]
pH plazmy
- PH 7.4 (7.36-7.44) › normální
- PH 7.0 › neutrální ale fatální!!!
MAC a Ca
Koncentrace ionizovaného vápníku
- Vazba vápníku na sérový albumin se snižuje s poklesem pH krve
- Snížení pH o 0,1 je spojeno se vzestupem Ca2+ přibližně o 0,03 mmol/l
- Pravděpodobně vliv i další faktory
- Inhibice syntézy vitaminu D
- Vliv na sekreci PTH
- Pufrační kostní mechanizmy
- Další